Oleh: Heru Setyawan
- Baterai timbal-asam: Karakteristik umum
- Baterai timbal-asam: Sejarah
- Baterai timbal-asam: Data pembuatan dan pemakaian baterai
- Baterai timbal-asam: Kimia (Karakteristik umum)
- Baterai timbal-asam: Kimia (Karakteristik tegangan sirkuit terbuka)
- Baterai timbal-asam: Kimia (Pemakaian sendiri)
- Baterai timbal-asam: Kimia (Karakteristik dan sifat asam sulfat)
Sebelum membahas tentang kehilangan tegangan, alangkah baiknya untuk mengingat kembali reaksi yang terjadi selama pemakaian dan pengisian baterai timbal-asam sebagai berikut:
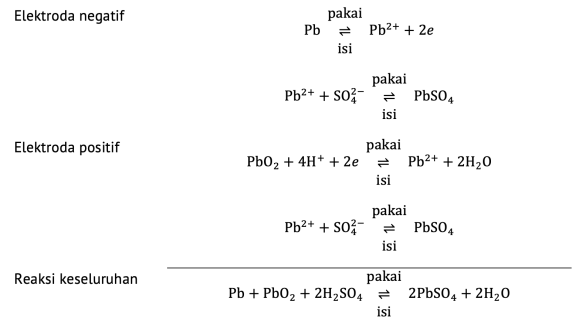
Ketika baterai sedang dipakai, tegangan pada pembebanan lebih rendah daripada tegangan sirkuit terbuka pada konsentrasi H2SO4 dan H2O yang sama dalam elektrolit dan Pb atau PbO2 dan PbSO4 dalam pelat. Keadaan stabil secara termodinamika untuk baterai adalah keadaan terpakai. Kerja (pengisian) harus dilakukan agar kesetimbangan reaksi elektrokimia pergi ke arah PbO2 pada positif dan Pb pada negatif. Jadi, tegangan sumber daya untuk pengisian kembali baterai timbal-asam harus lebih tinggi daripada tegangan Nernst dari baterai pada sirkuit terbuka.
Kurva pemakaian dan pengisian untuk elektroda positif dan negatif pada sel timbal-asam diilustrasikan pada Gambar 1. Begitu beban dikenakan, ada penurunan sesaat pada tegangan sel (region A). Pengaruh ini disebabkan oleh pembatasan elektrokinetika dan perpindahan massa dalam sel. Daerah miring pada kurva (region B) timbul dari kapasitas lapisan ganda. Hambatan dalam sel timbal-asam dalam keadaan terisi penuh mempunyai nilai dalam tingkan miliohm; nilai pastinya tergantung pada rancangan dan ukuran sel, metoda yang dipakai untuk pembuatan pelat, dan suhu. Hambatan sel meningkat selama pemakaian karena bahan pelat diubah menjadi timbal sulfat dan larutan elektrolit asamanya semakin menipis. Yang pertama diendapkan dalam pori-pori bahan aktif dan dengan begitu menghambat akses asam. Pengaruh penutupan pori-pori timbal adalah masalah khusus pada laju pemakaian tinggi. Penurunan suhu juga menghalangi difusi asam, dan selain itu, memperlambat aliran konveksi dengan meningkatkan viskositas larutan elektrolit.
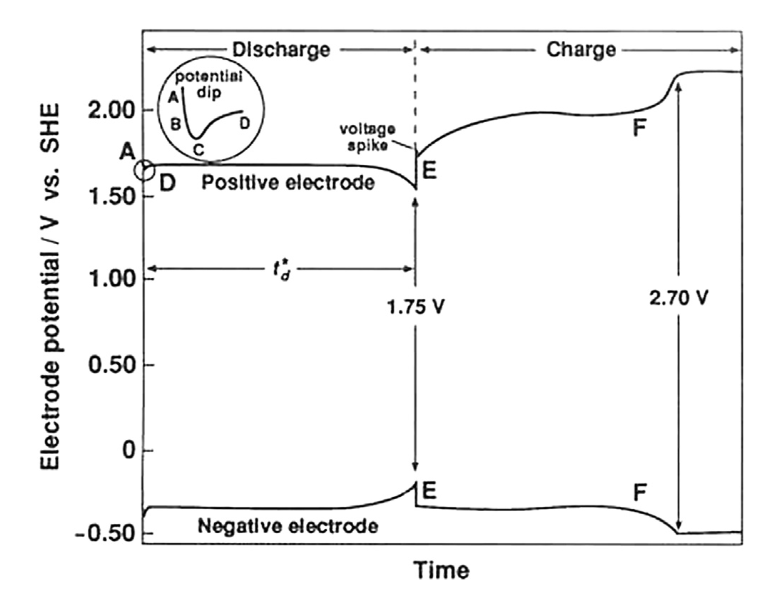
Potensial minimum pada kurva pemakaian (region C) dikenal sebagai “retakan lecutan” (whip crack). Fenomena ini disebabkan oleh perilaku pelat positif, lebih khusus, polimorf beta-PbO2 meskipun ada juga sumbangan dari elektroda negatif. Retakan lecutan lebih menonjol pada laju pemakaian tinggi, dengan kata lain, periode yang dibutuhkan untuk mencapai minimum lebih singkat, dan minimumnya sendiri lebih dalam. Penukikan tegangan disebabkan oleh adanya halangan karena nukleasi PbSO4 dalam pori-pori. Sebagai akibatnya, larutan dalam pori-pori dalam bahan aktif menjadi lewat jenuh dengan ion Pb2+. Ion Pb2+ akhirnya disingkirkan pada nilai minimum dari potensial elektroda. Laju pertumbuhan inti kristal PbSO4 pada keadaan ini menjadi lebih cepat daripada laju pembentukan ion sehingga potensial elektroda (dan dari sini tegangan sel) naik. Suatu keadaan akhirnya akan dicapai dimana reaksi elektrokimia dan nukleasi –> pertumbuhan kristal PbSO4 berlangsung pada laju yang sama dan potensial menjadi datar.
Dari uraian di atas dapat disimpulkan bahwa penyimpangan dari tegangan sirkuit terbuka selama pengisian atau pemakaian disebabkan, sebagian, karena kehilangan hambatan dalam baterai, dan sebagian, karena polarisasi. Kehilangan ini dapat diukur dengan memakai pemakaian terputus-putus, dimana kehilangan IR dapat diukur dengan hukum Ohm (E/I = R) dalam beberapa detik sampai beberapa menit setelah pemakaian dihentikan. Pengaruh polarisasi dapat membutuhkan waktu pengukuran beberapa jam untuk mengizinkan difusi di dalam pelat mencapai kesetimbangan kembali. Teknik spektroskopi impedansi bolak balik (alternating current; AC) juga berharga. Acuan standar hidrogen pada platina tidak praktis untuk sebagian besar pengukuran baterai timbal-asam, dan beberapa sistem elektroda acuan berbasis sulfat lain digunakan. Elektroda yang umum dipakai untuk pemeliharaan baterai adalah “batang” kadmium, tetapi ini secara khusus tidak stabil (+/-20 mV/hari). Elektroda acuan merkuri-merkurous sulfat adalah stabil dan tersedia dari beberapa vendor. Elektroda acuan Pb/H2SO4/PbO2 mengukur polarisasi pada pengisian dan pemakaian secara langsung, tanpa memerlukan koreksi koefisien panas yang berbeda dari electromotive force (emf). Perubahan polarisasi antara awal dan akhir pemakaian umumnya antara 50 sampai beberapa ratus mV, dan kapasitas sel dibatasi oleh kelompok pelat (positif atau negatif) yang mempunyai polarisasi terbesar selama pemakaian. Ketika perubahan kedua kelompok dalam sel sama, pembatasan kapasitas sepertinya lebih kepada penipisan H2SO4 dalam elektrolit daripada penipisan Pb atau PbO2 dalam pelat. Pada pengisian, polarisasi adalah ukuran yang baik bahwasanya kedua positif dan negatif telah diisi kembali: polarisasi pelat berubah lebih daripada 60 mV antara awal dan akhir pengisian kembali. Tegangan polarisasi menstabilkan pada beberapa harga ketika pelat diisi kembali dan gas dilepaskan secara bebas.
- Baterai timbal-asam: Karakteristik umum
- Baterai timbal-asam: Sejarah
- Baterai timbal-asam: Data pembuatan dan pemakaian baterai
- Baterai timbal-asam: Kimia (Karakteristik umum)
- Baterai timbal-asam: Kimia (Karakteristik tegangan sirkuit terbuka)
- Baterai timbal-asam: Kimia (Pemakaian sendiri)
- Baterai timbal-asam: Kimia (Karakteristik dan sifat asam sulfat)
Pustaka
A. Salkind & G. Zguris, Lead-Acid Batteries, dalam T. B. Reddy (Editor), Linden’s Handbook of Batteries, Edisi 4, McGraw-Hill, 2011.
J, Garce, E. Karden, P. T. Moseley, D. A. J. Rand, Lead-Acid Batteries for Future Automobiles, Elsevier, ed. 1, 2017.


Leave a comment